第二节 MHC抗原
一、HLA抗原的分子结构
1987年Bjorkman等首先借助X线晶体衍射技术弄清了HLA-A2分子的立体结构。其后,其它HLA-Ⅰ、Ⅱ类分子结构的研究也取得了进展,从而对这些分子的生物学功能提供了较确切的解释。
(一)HLA-Ⅰ类分子
所有的HLA-Ⅰ类分子均含有二条分离的多肽链,一条是由MHC基因编码的α链或称重链(44kD)。根据对HLA-A2和Aw68分子的晶体结构分析,Ⅰ类分子可分为四个区:(图5-5):①氨基端胞外多肽结合区:该区由二个相似的各包括90个氨基酸残基的片段组成,分别称为α1和α2。该功能区含有与抗原结合的部位。后者呈深槽状,其大小与形状适合于已处理的抗原片段,约容纳8~10个氨基酸残基。Ⅰ类分子的多态性残基也位于该区域。②胞外lg样区:该区又称为重链的α3片段,包括90个氨基酸残基,与免疫球蛋白的恒定区具有同源性。Ⅰ类分子与TC细胞表面CD8分子的结合部位即在α3片段。Ⅰ类分子的β链又称β2微球蛋白,也结合于该区。β链由第15号染色体的基因编码,它不插入细胞膜而游离于细胞外。β2微球蛋白与α1、α2、α3片段的相互作用对维持Ⅰ类分子于然构型的稳定性及其分子表达有重要意义。③跨膜区:该区氨基酸残基形成螺旋状穿过浆膜的脂质双层,将类分子锚定在膜上。④胞浆区:该区位于胞浆中,可能与细胞内外信息传递有关。
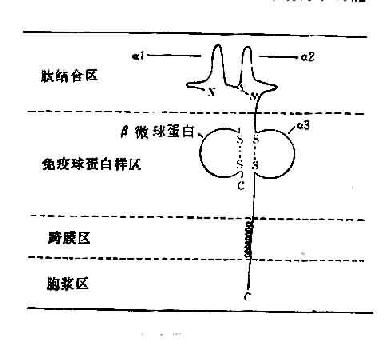
图5-5 HLA-Ⅰ类分子结构示意图
(二)HLA-Ⅱ类分子
所有的Ⅱ类分子均由二条以非共价键连接的多肽链(α、β)组成。二条链的基本结构相似,但分别由不同的MHC基因编码,且均具有多态性。虽然Ⅱ类分子的晶体衍射结构尚未得到,但光谱分析已证明与Ⅰ类分子具有某种相似性。Ⅱ类分子二条多肽链也可分为四个区,见(图10-6):①肽结合区:α链与β链的胞外部位均可再分为二个各含90个氨基酸残基的片段,分别称为α1、α2和β1、β2。肽结合区包括α1和β1片段,该二片段构成肽结合的裂隙(cleft),约可容纳14个氨基酸残基。Ⅱ类分子的多态性残基主要集中在α1和β1片段,这种多态性决定了多肽结合部位的生化结构,也决定了与肽类结合以及T细胞识别的特异性和亲和力。②lg样区:此区由α2和β2片段组成,两者均含链内二硫键,并属于lg基因超家族。在抗原呈递过程中,TH细胞的CD4分子与Ⅱ类分子结合的部位即位于该lg样非多肽态区域。③跨膜区和胞浆区:该二区与Ⅰ类分子α链的相应区域结构相似。
二、HLA抗原的组织分布
各类HLA抗原的组织分布不同。Ⅰ类抗原广泛分布于体内各种有核细胞表面,包括血小板和网织红细胞。除某些特殊血型者外,成熟的红细胞一般不表达Ⅰ类抗原。不同的组织细胞表达Ⅰ类抗原的密度各异。外周血白细胞和淋巴结、脾细胞所含Ⅰ类抗原量最多,其次为肝、皮肤、主动脉和肌肉。但神经细胞和成熟的滋养层细胞不表达Ⅰ类抗原。Ⅱ类抗原主要表达在某些免疫细胞表面,如B细胞、单核/巨噬细胞,树突状细胞,激活的t 细胞等,内皮细胞和某些组织的上皮细胞也可检出HLA-Ⅱ抗原。另外,某些组织细胞在病理情况下也可异常表达Ⅱ类抗原。Ⅰ、Ⅱ类抗原主要分布在细胞表面,但也可能现于体液中,血清、尿液、唾液、精液及乳汁中均已检出可溶性HLA-Ⅰ、Ⅱ类抗原。HLA-Ⅲ类抗原一般指几种补体成分,它们均分布于血清中。
三、HLA抗原表达的调控
在各类型细胞表面HLA分子表达与否以及表达的密度,可以受不同的因素调节。一般认为,调控HLA分子表达的主要环节是转录速率。可能影响HLA分子表达的因素有:①组织细胞的分化阶段:HLA分子是造血干细胞和某些免疫细胞的分化抗原,在细胞分化、成熟的不同阶段,各类HLA抗原的表达可有改变。例如HLA-DQ分子是人单核细胞的成熟标记;Ⅱ类抗原仅表达在激活的T细胞表面。②某些疾病状态:某些传染性疾病、免疫性疾病、造血系统疾病以及肿瘤均可影响HLA抗原表达。如AIDS病患者单核细胞HLA-Ⅱ类抗原表达明显减少,某些肿瘤细胞表面HLA-Ⅰ类抗原表达减少。③生物活性物质:某些细胞因子,例如三类干扰素(α、β、γ)以及TNFα、THFβ均可增强不同类型细胞HLA-Ⅰ类抗原表达;具有Ⅱ类抗原诱生能力的细胞因子包括IFNγ、TNFα、IL-6及GM-CSF等。此外,某些激素、某些神经递质和神经肽也可影响HLA分子表达。
HLA分子在免疫应答与免疫调节中是一类关键的分子,故各种因素对HLA分子表达的调控可能是体内免疫调节网络的重要组成部分。同时,受各种调节因子的影响,HLA分子的异常表达也参与某些疾病的发病机制。