第三节 药物消除动力学
从生理学看,体液被分为血浆、细胞间液及细胞内液几个部分。为了说明药动学基本概念及规律现假定机体为一个整体,体液存在于单一空间,药物分布瞬时达到平衡(一室模型)。问题虽然被简单化,但所得理论公式不失为临床应用提供了基本规律。按此假设条件,药物在体内随时间变化可用下列基本通式表达:dC/dt=kCn。C为血药浓度,常用血浆药物浓度。k为常数,t为时间。由于C为单位血浆容积中的药量(A),故C也可用A代替:dA/dt=kCn,式中n=0时为零级动力学(zero-order kinetics),n=1时为一级动力学(first-order kinetics),药物吸收时C(或A)为正值,消除时C(或A)为负值。在临床应用中药物消除动力学公式比较常用,故以此为例如以推导和说明。
一、零级消除动力学
当n=0时,-dC/dt=KC0=K(为了和一级动力学中消除速率常数区别,用K代k),将上式积分得:
Ct=C0- Kt,C0为初始血药浓度,Ct为t时的血药浓度,以C为纵座标、t为横座标作图呈直线(图3-6),斜率为K,当Ct/C0=1/2时,即体内血浆浓度下降一半(或体内药量减少一半)时,t为药物消除半衰期(half-life time, t1/2)。
按公式1/2C0=C0-Kt1/2
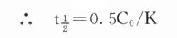
可见按零级动力学消除的药物血浆半衰期随C0下降而缩短,不是固定数值。零级动力学公式与酶学中的Michaelis-Menten公式相似:


图3-6 药物在体内消除过程的时量曲线
体内药物过多,超过机体最大消除能力(虚线)时为零级动力学恒速消除
体内药物降至虚线以下时为一级动力学恒比消除。插图纵坐标为对数标尺
二、一级消除动力学
当n=1时,-dC/dt=keC1=keC,式中k用ke表示消除速率常数 (elimination rate constant)。将上式积分得

可见按一级动力学消除的药物半衰期与C高低无关,是恒定值。体内药物按瞬时血药浓度(或体内药量)以恒定的百分比消除,单位时间内实际消除的药量随时间递减。消除速率常数(ke)的单位是h-1,它不表示单位时间内消除的实际药量,而是体内药物瞬时消除的百分率。例如ke=0.5h-1不是说每小时消除50%(如果t1/2=1小时则表示每小时消除50%)。按t1/2=0.693/ke计算t1/2=1.39h,即需1.39h后才消除50%。再按 计算,1小时后体内尚存60.7%。绝大多数药物都按一级动力学消除。这些药物在体内经过t时后尚存

当n=5时,At≈3%A0,即经过5个t1/2后体内药物已基本消除干净。与此相似,如果每隔一个t1/2给药一次(A0),则体内药量(或血药浓度)逐渐累积,经过5个t1/2后,消除速度与给药速度相等,达到稳态(steady state):

当n=5时,At≈97%A0。这一时间,即5个t1/2不因给药剂量多少而改变。具体数值见表3-2。
药物自体内消除的一个重要指标是血浆清除率(plasmaclearance,Cl),是肝肾等的药物消除率的总和,即单位时间内多少容积血浆中的药物被消除干净,单位用L・h-1(也有人用ml・min-1,和肌酐消除率一致)或按体重计算 L・kg-1・h-1。按定义,CL=RE/Cp,RE是消除速率(rate of elimination),即单位时间内被机体消除的药量,Cp为当时的血浆药物浓度。由于RE非固定值也不易检测,故常用表观分布容积(apparent volume ofdistribution, Vd)计算。 Vd是指静脉注射一定量(A)药物待分布平衡后,按测得的血浆浓度计算该药应占有的血浆容积。事实上静注药物后未待分布平衡已有部分药物自尿排泄及(或)在肝转化而消除,故必需多次检测Cp,作时量曲线图,将稳定下降的消除段向O时延升至和Y轴交点以求得理论上静注药量A在体内分布平衡时的血浆浓度C0,以此算出Vd=A/C0(图3-7)。按RE=keA,Cp=A/Vd,故Cl=keVd。在一级动力学的药物中,Vd及Cl是两个独立的药动学指标,各有其固定的数值,互不影响,也不因剂量大小而改变其数值。Vd是表观数值,不是实际的体液间隔大小。除少数不能透出血管的大分子药物外,多数药物的Vd值均大于血浆容积。与组织亲和力大的脂溶性药物其Vd可能比实际体重的容积还大。Cl也不是药物的实际排泄量。它反映肝和(或)肾功能,在肝和(肾)功能不足时Cl值会下降,因为Cl是肝肾等消除能力的总和。肝清除率虽然难测,但有重要的理论意义。肝清除率小的药物,首关消除少,其口服生物利用度大,但易受肝功能,血浆蛋白结合力及肝药酶诱导或抑制药的影响。肝清除率大的药物,首关消除多,其口服生物利用度小。有些药物的肝清除率很高,接近肝血流量,称为灌流限制性清除,其肝清除率受肝血流量影响较大。药物以原形自肾消除的百分率比较容易测定。自肾排泄多的药物易受肾功能影响,自肾排泄少的药物易受肝功能影响。医生可以据此在肝或肾功能不足病人适当调整剂量。在零级动力学的药物中,RE以恒速消除,不随Cp下降而改变,故Cl 值不固定,与Cp成反比。

图3-7 表观分布容积计算法
C0是静注药量A在0时理论上的血药浓度
Cl值实际上常用静脉或肌肉注射药物A后测定Cp,绘出时量曲线,算出AUC再按CL=A/AUC取得。因为AUC=C0/ke,代入得
CL=keVd=C0Vd/AUC=A/AUC。
三、连续恒速给药
临床治疗常需连续给药以维持有效血药浓度。在一级动力学药物中,开始恒速给药时药物吸收快于药物消除,体内药物蓄积。按 计算约需5个t1/2达到血药稳态浓度(Css)(图3-8),此时给药速度(RA)与消除速度(RE)相等。
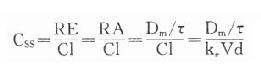
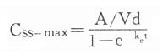
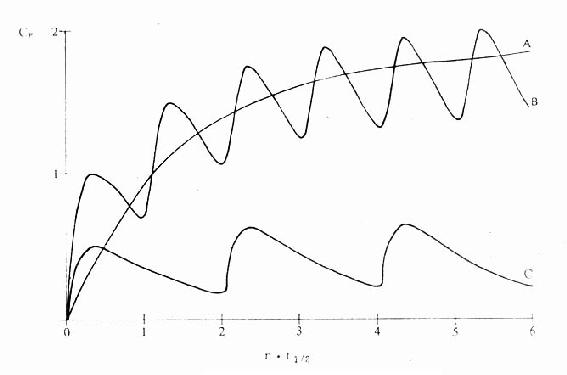
图3-8 连续恒速给药时的时量曲线
约经5个半衰期血药浓度达到稳态。给药间隔越短,
血药浓度波动越小。给药剂量越大,血药浓度越高
A.静脉滴注,Dm/t1/2B.肌肉注射,Dm/t1/2
C.肌肉注射,1/2Dm/2t1/2。Dm维持剂量
但从调整剂量时开始需再经过5个t1/2方能达到需要的Css。
在病情危重需要立即达到有效血药浓度时,可于开始给药时采用负荷剂量(loading dose,D1),因为
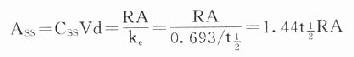
Ass就是负荷剂量。可将第一个t1/2内静脉滴注量的1.44倍在静脉滴注开始时推注入静脉即可立即达到并维持Css。在分次恒速给药达到Css时,体内Ass是维持剂量(maintenance dose, Dm)与体内上一剂量残留药物的和,即

当给药间隔时间τ=t1/2时,

即每隔一个t1/2给药一次时采用首剂加倍剂量的D1可使血药浓度迅速达到Css。
理想的给药方案应该是使CSS- max略小于最小中毒血浆浓度(MTC)而CSS-min略大于最小有效血浆浓度(MEC),即血药浓度波动于MTC与MEC之间治疗窗,这一Dm可按下列公式计算:
Dm=(MTC - MEC)Vd
负荷剂量计算法与上同,即D1=ASS=1.44t1/2 RA=1.44t1/2 Dm/τ,τ为给药间隔时间。τ可按一级消除动力学公式推算得

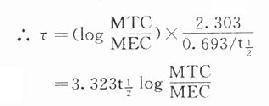
因此可以根据药物的MTC及MEC利用这些公式计算出D1,Dm及τ。注意此时τ≠t1/2,D1≠2Dm(图3-9)。
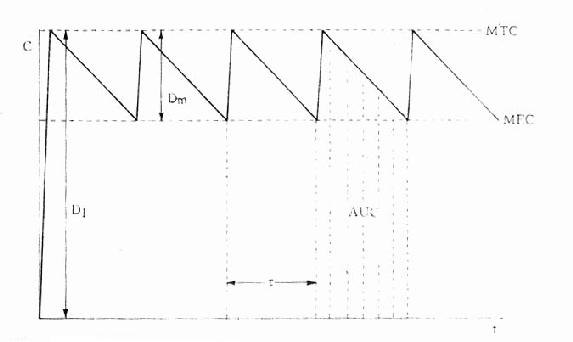
图3-9 负荷剂量、维持剂量、给药间隔与血药浓度关系
Dm维持剂量所形成的C D1负荷剂量所形成的C
在零级动力学药物中,体内药量超过机体最大消除能力。如果连续恒速给药,RA>RE,体内药量蓄积,血药浓度将无限增高。停药后消除时间也较长,超过5个t1/2。因为t1/2=0.5C0/K,达到C0越高t1/2越长。
临床用药可根据药动学参数如Vd、Cl、ke、t1/2及AUC等按以上各公式计算剂量及设计给药方案以达到并维持有效血药浓度。除了少数t1/2特长或特短的药物,或零级动力学药物外,一般可采用每一个半衰期给于半个有效量(half dose athalf life interval)并将首次剂量加倍是有效、安全、快速的给药方法。
有些药在体内转化为活性产物则需注意此活性产物的药动学,如果活性产物的消除是药物消除的限速步骤的话,则应按该产物的药动学参数计算剂量及设计给药方案。
四、一级药动学指标间的相互关系
1.F=A/D×100%口服剂量(D)由于不能100%吸收及存在首关消除效应,能进入体循环的药量(A)只占D的一部分,这就是生物利用度(F)。药动学计算时应采用绝对生物利用度,相对生物利用度作为评比药物制剂质量的指标。生物利用度还包括吸收速度问题,达峰时间(Tpeak)是一个参考指标。
2.A=C・Vd或C=A/Vd体内药量(A)与血药浓度(C)比值固定,在许多药动学公式中,A与C可以通用,如At=也可用Ct=。
3.Cp=[D]+[DP] 血浆中药物有游离型(D)与血浆蛋白结合型(DP),定量测定时需将血浆蛋白沉淀除去,故通常所说的血浆药物浓度(Cp)是指[D]与[DP]的总和。只有透析法或超离心法才可能将二者分离以计算药物的血浆蛋白结合率
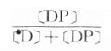
4.
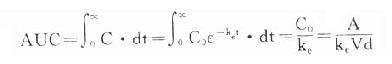
5.ke=0.693/t1/2=RE/A=CL/Vd消除速率常数是药物瞬时消除的百分率而不是单位时间药物消除速率(RE),是决定t1/2的参数,但其本身又取决于Cl及Vd,故不是独立的药动学指标。
6.Vd=A/C0=A/AUC ke 表现分布容积(Vd)是独立的药动学指标,不是实际的体液容积,取决于药物在体液的分布。Vd大的药物与组织蛋白结合多,主要分布于细胞内液及组织间液。Vd小的药物与血浆蛋白结合多,较集中于血浆。Vd不因A多少而变化。
7.CL=keVd=RE/Cp=A/AUC 血浆清除率(Cl)是肝肾等清除率的总和,也不是实际的药物消除速率(RE),是另一个独立于A的重要药动学指标,但受肝肾功能的影响。
8.t1/2=0.693/ke=0.693Vd/CL 血浆药物消除半衰期(t1/2)是一个非常实用的药动学指标,虽然独立于A,但受Cl及Vd双重制约,Cl大时t1/2短,Vd大时t1/2长。例如庆大霉素Cl小(60ml・min-1),Vd也小(0.25L・kg-1),其t1/2不长(2~3h)。氯喹Cl大(700ml・min-1),Vd也大(185L・kg-1),其t1/2并不短(8天)。药物在吸收及分布过程中也有半衰期,分别用t1/2a及t1/2α表示。
9.稳态时RA=RE=CSS・Cl=CSS・Vd・ke
故

10.

11.
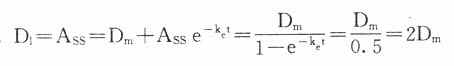
五、房室模型
以上所述各种药动学公式都是将机体视为一个整体空间,假设药物在其中转运迅速,瞬时达到分布平衡的条件下推导而得的。实际上机体绝非如此简单,不仅有血浆、细胞外液及细胞内液等间隔,而且各组织细胞间存在着无数的区间。静脉注射药物的时量(对数标尺)关系并非直线,而是一条由无数区段组成的连续弧线。粗略地看可见早期一段快速下降,后来才逐渐稳定缓慢下降。这是因为药物进入血液循环后快速向组织分布,首先进入血注量大的肺、肾、心、脑等器官,然后再向其他组织分布,最后达到平衡(假平衡)。因此设想机体由几个互相连通的房室(compartment)组成。这个房室不是解剖学上分隔体液的房室,而是按药物分布速度以数学方法划分的药动学概念。多数药物按二房室模型转运(少数单房室或多房室),中央室大致包括血浆及那些血流量多的器官,周边室包括机体其余部分,界限并不明确。时量曲线因此也只能大致分为分布相及消除相两个指数衰减区段(图3-10)。其药动学规律与单房室不同,如C=Ae-αt +Be-βt,α及β分别为分布相(A)及消除相(B)的消除速率常数。而且在分布相中Vd逐渐增大,ke(α)逐渐减少,t1/2逐渐延长,因此药动学计算需要特殊处理。即使在消除相,血药浓度稳定线性下降,各组织浓度及其下降速度也不尽相等,故称假平衡。可见问题非常复杂。
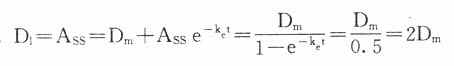
图3-10 二房室模型时量曲线
A.分布相(实线)及分布曲线(虚线)
B.消除相(实线)与消除曲线(虚线)
正由于问题过于复杂,临床应用诸多不便,实际运算也存在诸多困难。房室模型并非药物固有的药动学指标,机体也无此解剖学间隔,即使运用电子计算机拟合也不一定获得明确的划分。用同一药物试验,在某些人呈二室模型,另些人可能呈一室或三室模型。同一药物静脉注射时呈二室模型而口服则呈单一房室模型。在分布相时药物实际上已开始消除,到达消除相时可能已有相当分量的药物已被消除。如果用血管外给药(口服、肌注等)分布相常被吸收相掩盖。这些时相的划分仅靠血药浓度的测定。如果早期(此时血药浓度变化较快)取样间隔过疏,很难据此准确划分时相,因此,越来越多的临床家及研究者逐渐放弃房室模型而转向采用适用于所有药物的无房室方法(noncompartmentalmedtod)来解决实际问题,对此,有待今后深入学习。
从另一方面看,时量曲线在达到假平衡后已呈单一指数衰减的直线,此时房室划分已无需要,可以按β值计算t1/2及其他实用的药动学指标。
AUC是与房室无关的药动学指标,可用实验方法测定。AUC(0-∞)=C0/ke,或AUC(T-∞)=CT/β,T是消除相开始的时间。再用AUC算出Vd及Cl:
Vd=A/AUCβ,CL=A/AUC