第二节 血脂及其代谢
血浆中含有的脂类统称为血酯,包括甘油三酯、磷脂、胆固醇及其酯和非酯化脂肪(nonesterified fatty acid),亦称游离脂肪酸(free fatty acid,简写FFA)。血脂在脂类的运输和代谢上起着重要作用。血脂只占体重的0.04%,其含量受到饮食、营养、疾病等因素的影响,因而是临床上了解患者脂类代谢情况的一个重要窗口。正常人血脂含量见表5?。它们是以脂蛋白的形式存在并运输的,脂蛋白由脂类与载脂蛋白结合而形成。脂蛋白具有微团结构,非极性的甘油三酯、胆固醇酯等位于核心,外周为亲水性的载脂蛋白和胆固醇磷脂等的极性基因,这样使脂蛋白具有较强水溶性,可在血液中运输(图5-2)。
表5-1 正常成人空腹血脂的主要成分和含量
| 脂类物质 | 含量(毫克/100毫升血浆) | 脂类物质 | 含量(毫克/100毫升血浆) |
| 脂类总重 | 400-700(500) | 胆固醇 | 105-260(200) |
| 甘油三酯 | 10-160(100) | 酯型 | 90-260(145) |
| 磷脂 | 150-250(200) | 自由型 | 40-70(55) |
| 磷脂酰胆碱 | 80-225(110) | 脂肪酸总量 | 110-485(300) |
| 磷脂酰乙醇胺 | 0-30(10) | 非酯化型化脂肪酸 | 5-20 |
| 神经磷脂 | 10-50(30) |
注:括弧内为平均值
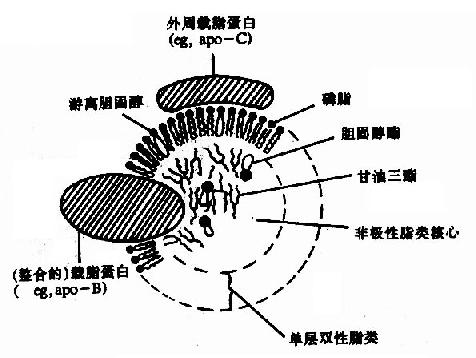
图5-2 血浆脂蛋白的一般结构
一、血浆脂蛋白的分类
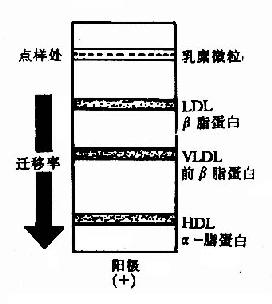
图5-3 血浆脂蛋白的电泳行为
血液中的脂蛋白不是单一的分子形式,其脂类和蛋白质的组成有很大的差异,因此血液中的脂蛋白存在多种形式。根据它们各自的特性采用不同的分类方法,可将它们进行多种分类,一般采用电泳法和超速离心法进行血浆脂蛋白的分类。
(一)电泳分类法
本法根据不同脂蛋白所带表面电荷不同,在一定外加电场作用下,电泳迁移率不同,可将血浆脂蛋白分为四类。如以硝酸纤维素薄膜为支持物,电泳结果是:α-脂蛋白泳动最快,相当于α1-球蛋白的位置;前β脂蛋白次之,相当于α2-球蛋白位置;β-脂蛋白泳动在前-β之后,相当于β-球蛋白的位置;乳糜微粒停留在点样的位置上(见图5-3)。
(二)超速离心法
本法依据不同脂蛋白中蛋白质脂类成分所占比例不同,因而分子密度不同(甘油三酯含量多者密度低,蛋白质含量多的分子密度高),在一定离心力作用下,分子沉降速度或漂浮率不同,将脂蛋白分为四类,即乳糜微粒(chylomicrons)、极低密度脂蛋白(very low densitylipoprotein,VLDL)、低密度脂蛋白(lowdensity lipoprotein,LDL)和高密度脂蛋白(highdensitylipoprotein,HDL);分别相当于电泳分离中的乳糜微粒、前β脂蛋白、β脂蛋白和α脂蛋白。除上述几类脂蛋白以外,还有一种中间密度脂蛋白(intermediate density lipoprotein,IDL)其密度位于VLDL与LDL之间,这是VLDL代谢的中间产物。HDL在代谢过程中分子中蛋白与脂类成分有变化,可将HDL再分为HDL1、HDL2与HDL3。HDL1是在高胆固醇膳食时才出现,HDL2为成熟的HDL,HDL3为新生的HDL,其分子中蛋白成分多。
血浆中的游离中短链脂肪酸可与血浆白蛋白结合而被运输,称之为脂酸白蛋白。由于脂类染色时脂肪酸不着色,所以不易观察,实际上它的位置与白蛋白相当。
二、血浆脂蛋白的组成
(一)脂蛋白中脂类的组成特点:
除脂酸白蛋白外,各类脂蛋白均含有甘油三酯、磷脂、胆固醇及其酯。但组成比例有很大差异,其中甘油三酯在乳糜微粒中含量为最高,达其化学组成的90%左右。磷脂含量以HDL为最高,达40%以上。胆固醇及其酯以LDL中最多,几乎占其含量50%。VLDL中以甘油三酯含量为最多,达60%(见表5-2)。
表5-2 血浆脂蛋白的组成
| 组成 | |||||||||||||
| 分类 | 密度 | 颗粒直径 | S1 | 电泳 | 蛋白质 | 总脂 | 占总脂的% | 合成 | 功能 | ||||
| (mm) | 位置 | 甘油 | 胆固 | 游离 | 部位 | ||||||||
| % | % | 磷脂 | 胆固醇 | ||||||||||
| 三酯 | 醇 酯 | 脂肪酸 | |||||||||||
| CM | <0.95 | 90- | >400 | 原点 | 1-2 | 98-99 | 88 | 8 | 3 | 1 | 小肠粘 | 转运外源性情 | |
| 1000 | 膜细胞 | 甘油三酯 | |||||||||||
| VLDL | 0.95- | 30- | 20- | α2球 | 7-10 | 90-93 | 56 | 20 | 15 | 8 | 1 | 肝细胞 | 转运内源性 |
| 前β脂蛋白 | 1.006 | 90 | 400 | 蛋白 | 甘油三酯 | ||||||||
| LDL | 1.006- | 20-25 | 2-20 | β球 | 21 | 79 | 13 | 28 | 48 | 10 | 1 | 血浆 | 转运内源性 |
| β脂蛋白 | 1.063 | 蛋白 | 胆固醇 | ||||||||||
| HDL | 1.063- | 12-20 | 沉降 | α1球 | 33 | 67 | 16 | 43 | 61 | 10 | 4 | 肝肠 | 转运外源 |
| α脂蛋白 | 1.125 | 蛋白 | 血浆 | 性胆固醇 | |||||||||
| HDL2 | 1.125 | 7.5-10 | 沉降 | α1球 | 57 | 43 | 13 | 46 | 29 | 6 | 6 | 肝肠 | 转运内源性 |
| HDL3 | 1.120 | 蛋白 | 血浆 | 胆固醇 | |||||||||
(二)载脂蛋白(apoprotein,apo)
脂蛋白中与脂类结合的蛋白质称为载脂蛋白,载脂蛋白在肝脏和小肠粘膜细胞中合成。目前已发现了十几种载脂蛋白,结构与功能研究比较清楚的有apoA、apoB、apoC、apoD与apoE五类。每一类脂蛋白又可分为不同的亚类,如apoB分为B100和B48;apoC分为CⅠ、CⅡ、CⅢ等。载脂蛋白在分子结构上具有一定特点,往往含有较多的双性α-螺旋结构,表现出两面性,分子的一侧极性较高可与水溶剂及磷脂或胆固醇极性区结合,构成脂蛋白的亲水面,分子的另一侧极性较低可与非极性的脂类结合,构成脂蛋白的疏水核心区。
载脂蛋白的主要功能是稳定血浆脂蛋白结构,作为脂类的运输载体。除此以外有些脂蛋白还可作为酶的激活剂:如apoAI激活卵磷脂胆固醇脂酰转移酶(lecithincholesteroltransferase.LCAT),apoCⅡ可激活脂蛋白脂肪酶(lipoproteinlipase,LPL)。有些脂蛋白也可作为细胞膜受体的配体:如apo B-48,apoE参与肝细胞对CM的识别,apoB-100可被各种组织细胞表面LDL受体所识别等(见表5-3)。
表5-3 血浆脂蛋白的载脂蛋白
| 载脂蛋白 | 脂蛋折 | 氨基酸数 | 分子量 | 来源 | 功能 | 含量 |
| AⅠ | HDL,CM | 243 | 28.300 | 肝、肠 | 激活LCAT;HDL受体配基 | 121.8±13.7* |
| AⅡ | HDL,CM | 77 | 17.500 | 肝、肠 | 稳定HDL结构?抑制LCAT? | 33.0±5.0* |
| AⅣ | CM,HDL | 371 | 46.000 | 肠 | 功能不清(促进CM合成?) | 17±2△ |
| B-100 | LDL,VLDL,IDL | 4536 | 512,723 | 肝 | LDL受体配基(识别LDL受体) | 87.3±143* |
| B-48 | CM,CM残粒 | 265 000 | 肠 | 促进CM合成 | 5△ | |
| CⅠ | VLDL,HDL,CM | 57 | 6,500 | 肝 | 激活LCAT? | 7.8±2.4* |
| CⅡ | VLDL,HDL,CM | 79 | 8,800 | 肝 | 激活肝外LPL | 5.0±1.8* |
| CⅢ | VLDL,HDL,CM | 79 | 8,900 | 肝 | 抑制LPL,抑制肝apoE受体 | 11.8±3.6* |
| D | HDL | 22,100 | 肝? | 功能不清(转达运胆固醇酯? | 10±4△ | |
| VLDL,HDL,CM | LDL受体配基,肝CM残受体) | |||||
| E | CM残粒 | 299 | 34,000 | 肝 | (apoE受体)配基 | 3.5±1.2* |
*华西医科大学生化教研室对625例成都地区正常成人测定的结果。△国外报导参考值。
LCAT:卵磷脂胆固醇脂酰转移酶 LPL:脂蛋白脂肪酶
(三)脂蛋白的代谢
1.乳糜微粒(CM)
乳糜微粒是在小肠粘膜细胞中生成的,食物中的脂类在细胞滑面内质网上经再酯化后与粗面内质网上合成的载脂蛋白构成新生的(nascent)乳糜微粒(包括甘油三酯、胆固醇酯和磷脂以及poB48),经高尔基复合体分泌到细胞外,进入淋巴循环最终进入血液。
新生乳糜微粒入血后,接受来自HDL的apoC和apoE,同时失去部分apoA,被修饰成为成熟的乳糜微粒。成熟分子上的apoCⅡ可激活脂蛋白脂肪酶(LPL)催化乳糜微粒中甘油三酯水解为甘油和脂肪。此酶存在于脂肪组织、心和肌肉组织的毛细血管内皮细胞外表面上。脂肪酸可被上述组织摄取而利用,甘油可进入肝脏用于糖异生。通过LPL的作用,乳糜微粒中的甘油三酯大部分被水解利用,同时apoA、apoC、胆固醇和磷脂转移到HDL上,CM逐渐变小,成为以含胆固醇酯为主的乳糜微粒残余颗粒(remnant)。肝细胞膜上的apoE受体可识别CM残余颗粒,将其吞噬入肝细胞,与细胞溶酶体融合,载脂蛋白被水解为氨基酸,胆固醇酯分解为胆固醇和脂肪酸,进而可被肝脏利用或分解,完成最终代谢(图5-4)。
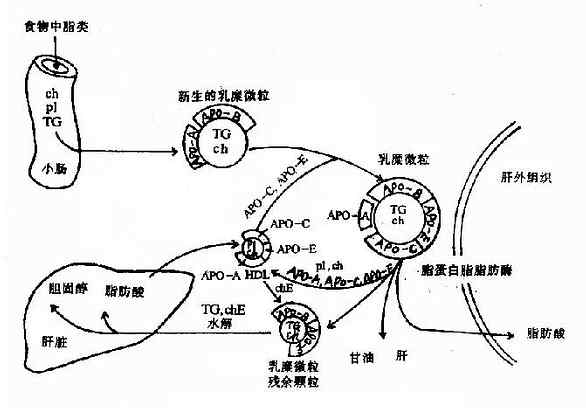
图5-4 乳糜微粒(CM)的代谢过程
TG:甘油三酯;pL:磷脂;Ch:胆固醇;ChE:胆固醇酯;ApO:载脂蛋白;HDL:高密度脂蛋白。
由此可见,CM代谢的主要功能就是将外源性甘油三酯转运至脂肪、心和肌肉等肝外组织而利用,同时将食物中外源性胆固醇转运至肝脏。
2.极低密度脂蛋白(VLDL)
VLDL主要在肝脏内生成,VLDL主要成分是肝细胞利用糖和脂肪酸(来自脂动员或乳糜微粒残余颗粒)自身合成的甘油三酯,与肝细胞合成的载脂蛋白apoB100、apoAI和apoE等加上少量磷脂和胆固醇及其酯。小肠粘膜细胞也能生成少量VLDL。
VLDL分泌入血后,也接受来自HDL的apoC和apoE:apoCⅡ激活LPL,催化甘油三酯水解,产物被肝外组织利用。同时VLDL与HDL之间进行物质交换,一方面是将apoC和apoE等在两者之间转移,另一方面是在胆固醇酯转移蛋白(cholesteryl ester transfer protein)协助下,将VLDL的磷脂、胆固醇等转移至HDL,将HDL的胆固醇酯转至VLDL,这样VLDL转变为中间密度脂蛋白(IDL)。IDL有两条去路:一是可通过肝细胞膜上的apoE受体而被吞噬利用,另外还可进一步入被水解生成LDL(图5-5)。
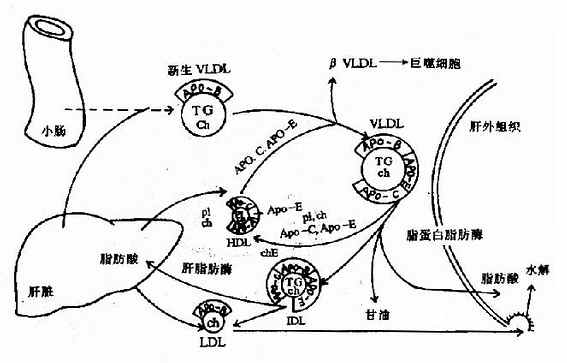
图5-5 极低密度脂蛋白(VLDL)的代谢过程
IDL:中间密度脂蛋白;LDL:低密度脂蛋白;
由此可见,VLDL是体内转运内源性甘油三酯的主要方式。
3.低密度脂蛋白(LDL)
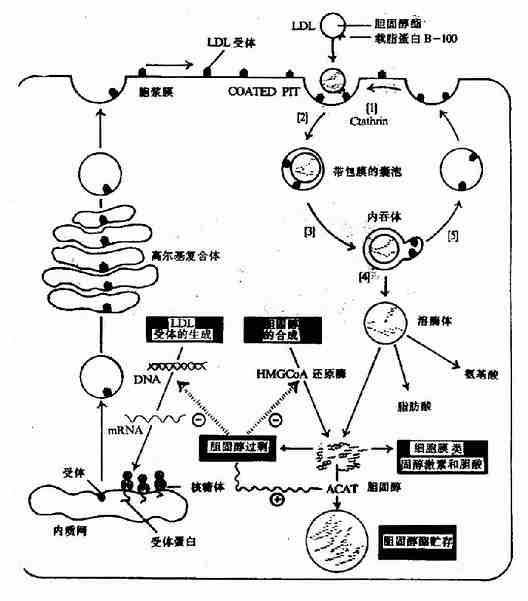
图5-6 细胞对LDL的摄取和降解
LDL由VLDL转变而来,LDL中主要脂类是胆固醇及其酯,载脂蛋白为apoB100。
LDL在血中可被肝及肝外组织细胞表面存在的apoB100受体识别,通过此受体介导,吞入细胞内,与溶酶体融合,胆固醇酯水解为胆固醇及脂肪酸。这种胆固醇除可参与细胞生物膜的生成之外,还对细胞内胆固醇的代谢具有重要的调节作用:①通过抑制HMGCoA还原酶(HMGCoa reductase)活性,减少细胞内胆固醇的合成;②激活脂酰CoA胆固醇酯酰转移酶(acyl CoA:cholesterol acyltransferase,ACAT)使胆固醇生成胆固醇酯而贮存;③抑制LDL受体蛋白基因的转录,减少LDL受体蛋白的合成,降低细胞对LDL的摄取(图5-6)。
除上述有受体介导的LDL代谢途径外,体内内皮网状系统的吞噬细胞也可摄取LDL(多为经过化学修饰的LDL),此途径生成的胆固醇不具有上述调节作用。因此过量的摄取LDL可导致吞噬细胞空泡化。
从以上可以看出,LDL代谢的功能是将肝脏合成的内源性胆固醇运到肝外组织,保证组织细胞对胆固醇的需求。
4.高密度脂蛋白(HDL)
HDL在肝脏和小肠中生成。HDL中的载脂蛋白含量很多,包括apoA、apoC、apoD和apoE等,脂类以磷脂为主。
HDL分泌入血后,新生的HDL为HDL3,一方面可作为载脂蛋白供体将apoC和apoE等转移到新生的CM和VLDL上,同时在CM和VLDL代谢过程中再将载脂蛋白运回到HDL上,不断与CM和VLDL进行载脂蛋白的变换。另一方面HDL可摄取血中肝外细胞释放的游离胆固醇,经卵磷脂胆固醇酯酰转移酶(LCAT)催化,生成胆固醇酯。此酶在肝脏中合成,分泌入血后发挥活性,可被HDL中apoAI激活,生成的胆固醇酯一部分可转移到VLDL。通过上述过程,HDL密度降低转变为HDL2。HDL2最终被肝脏摄取而降解(图5-7)。
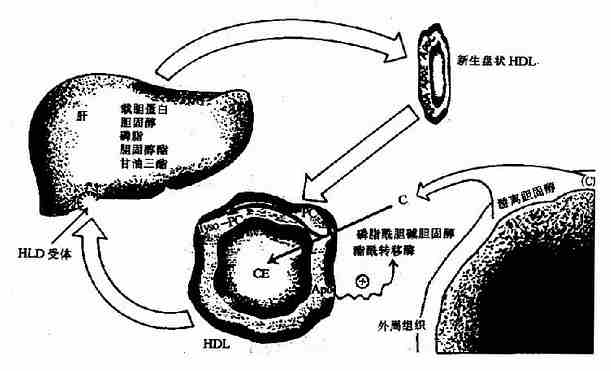
图5-7 HDL代谢 PC表示磷脂酰胆碱,LysoPC表示溶解性磷脂酰胆碱
由此可见,HDL的主要功能是将肝外细胞释放的胆固醇转运到肝脏,这样可以防止胆固醇在血中聚积,防止动脉粥样硬化,血中HDL2的浓度与冠状动脉粥样硬化呈负相关。
(四)高脂蛋白血症
血浆脂蛋白代谢紊乱可以表现为高脂蛋白血症和低脂蛋白血症,后者较为少见,现只介绍高脂蛋白血症。
高脂蛋白血症(hyperlipoproteinemia)亦称高脂血症(hyperlipidemia),因实际上两者均系血中脂蛋白合成与清除紊乱所致。这类病症可以是遗传性的,也可能是其他原因引起的,表现为血浆脂蛋白异常、血脂增高等,现将其六种主要类型列于表5-4。
表5-4 高脂蛋白血症的类型
| 类型 | 脂蛋白变化 | 血脂的变化 | ||
| 主要升高的脂类 | 次要升高的脂类 | 病因 | ||
| Ⅰ | CM增高 | 甘油三酯 | 胆固酯 | LPL或apoCⅡ遗传缺陷 |
| Ⅱa | LDL增高 | 胆固醇 | LDL受体的合成或功能的遗传缺陷 | |
| Ⅱb | LDL VLDL增高 | 甘油三酯 | 胆固醇 | 遗传因素影不大,主要受膳食影响 |
| Ⅲ | LDL增高 | 甘油三酯胆固醇 | apoE异常于扰了CM及VLDL残粒的吸收 | |
| Ⅳ | VLDL增高 | 甘油三酯 | 胆固醇 | 分子缺陷不清,多由于肥胖,饮酒过量或糖尿病所致 |
| Ⅴ | CM VLDL增高 | 甘油三酯 | 胆固醇 | 实际为型Ⅰ和Ⅳ型的混合症 |